ペーシング(電気刺激) により、心筋細胞の拍動レートをコントロールすることができます。拍動レートを一定化することにより、使用依存性(例 : 拍動レート依存性)化合物の評価などが可能になります。また、オプトジェネティクスでは、特定因子への刺激や、アーチファクト無しのデータ測定など、より精度の高い心筋細胞アッセイが行えます。
Maestro MEAは、電気刺激の印加が可能です。また、光刺激装置 LUMOS を用いて光照射によるペーシングも可能です。拍動レートのコントロールは、well 間及びプレート間差を抑制するなど、心筋細胞アッセイの精度を向上させます。
ペーシングによるアッセイ品質・再現性の向上
化合物の誘発よる心筋細胞の Field potential duration (FPD) 変化の検証は、新薬の安全性評価試験において広く用いられています。しかしながら、心筋細胞の再分極のタイミングは拍動レートと連動し、FPDは拍動レートの変化によっても変化します。ペーシングによる拍動レートの一定化は、拍動レートによる FPD 変化を排除します。また、well 間差、アッセイ間差を抑制し、アッセイの精度を向上させます。
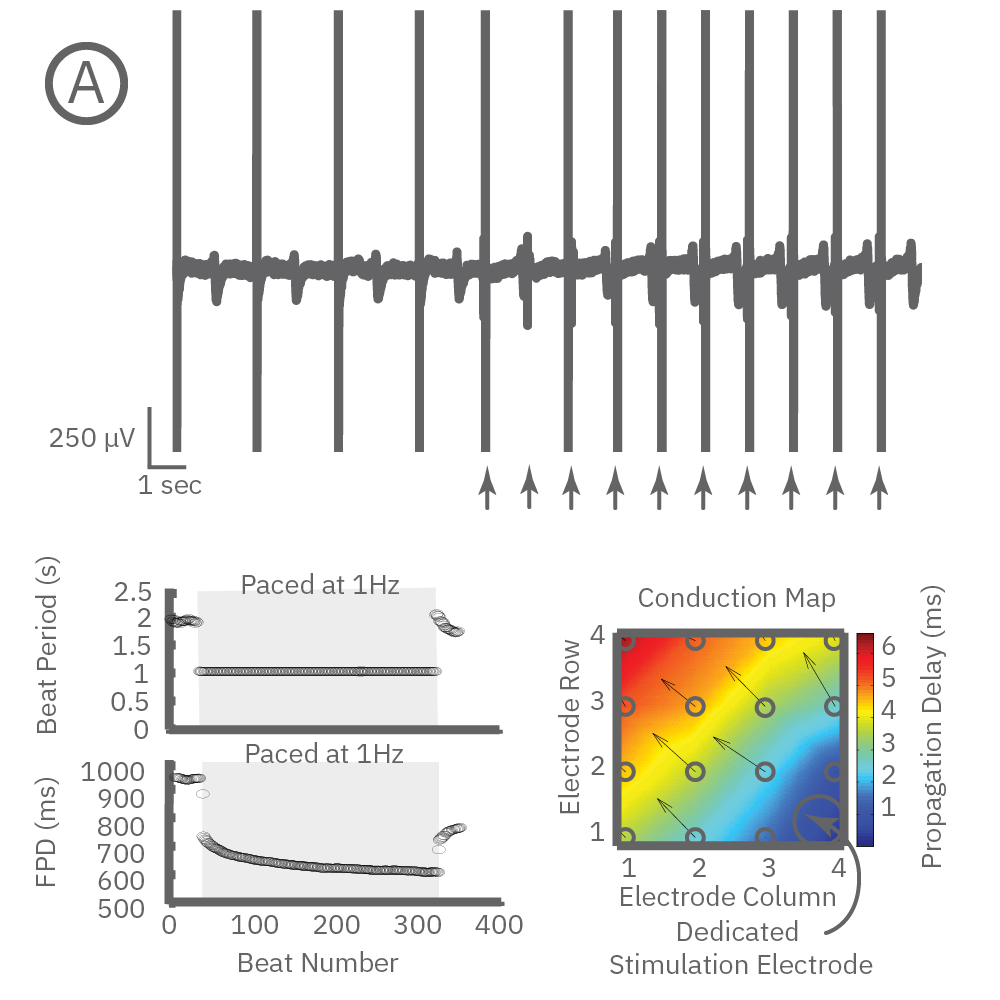
(A) 電気 (或いは光)ペーシング下で得られた心筋細胞の応答波形と各解析結果。上図は測定された生波形で、矢印はペーシングの印加を示す。左下段は拍動間隔 (Beat Period) 及び FPD (Field Potential Duration) の変化、右下段はシグナル伝播を示す。
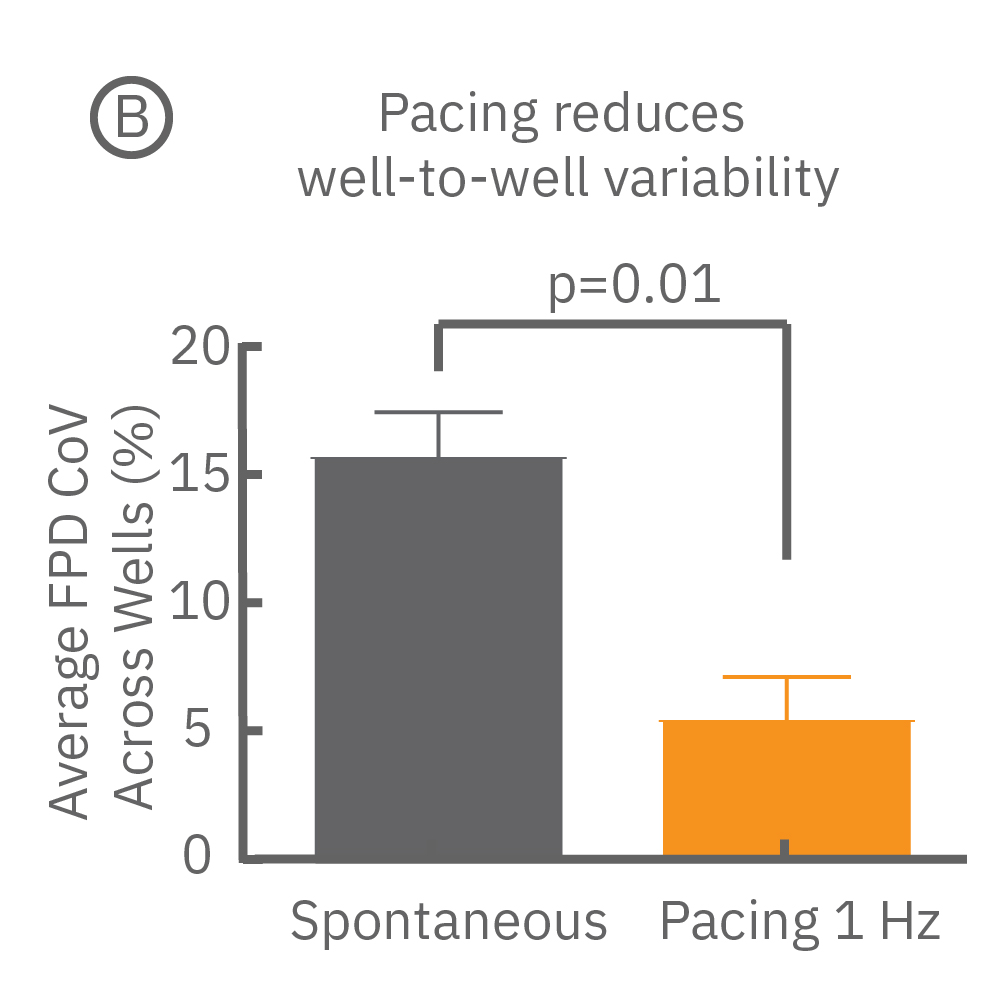
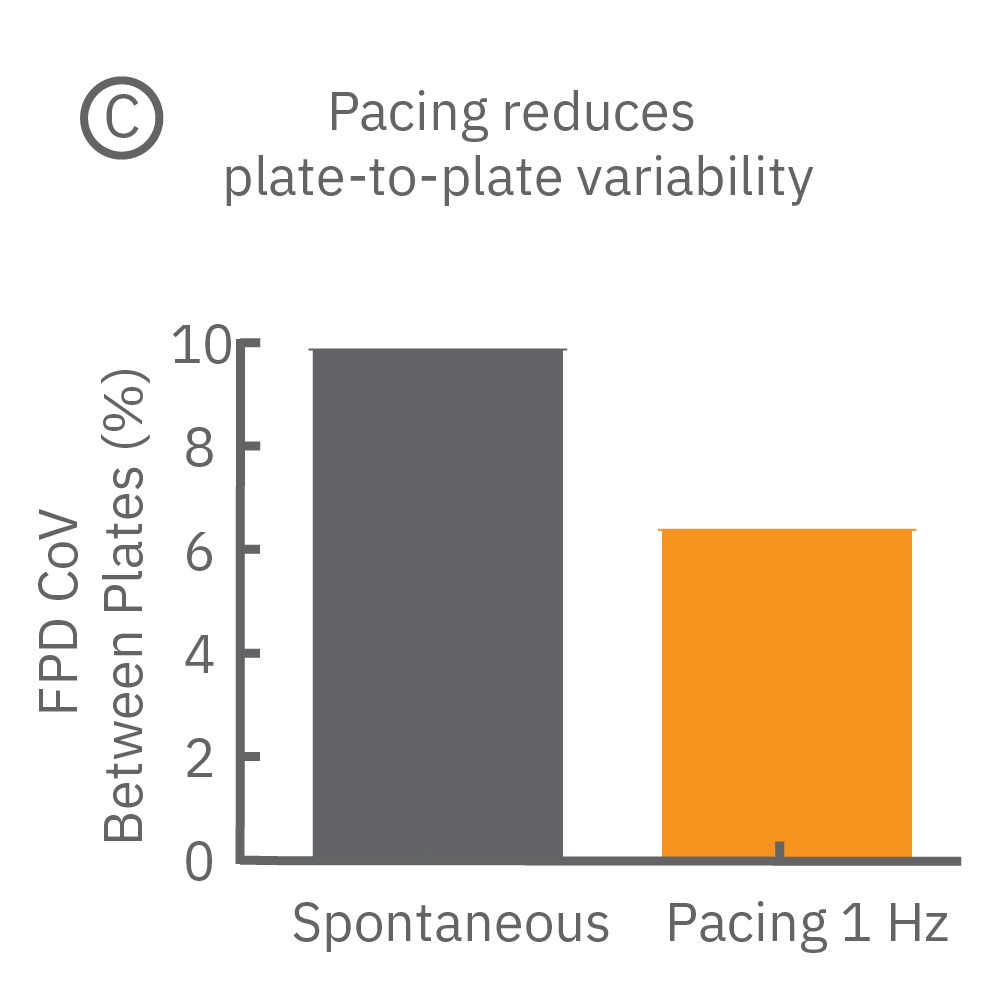
(B,C) Pluricyte® 心筋細胞から得られた、自発応答時とペーシング応答時におけるWell毎 (B)、及びプレート毎(C)の変動係数 (CoV)。ペーシングにより、Well 間のFPDのばらつきは大きく減少した(p=0.01、B)。また、プレート間のばらつきにも減少が得られた。
拍動レート制御による検証
化合物には、使用依存性を示すものが多くあります。拍動レートの遅延時に強い効果を示す「逆使用依存性」は、催不整脈リスクの重要な指標の1つです。一部の Maestro MEA プレートには大容量刺激印加が可能な電極が装着されています。心筋細胞へのペーシングにより自在に拍動レートをコントロールし、このような依存的効果を検証することが可能です。
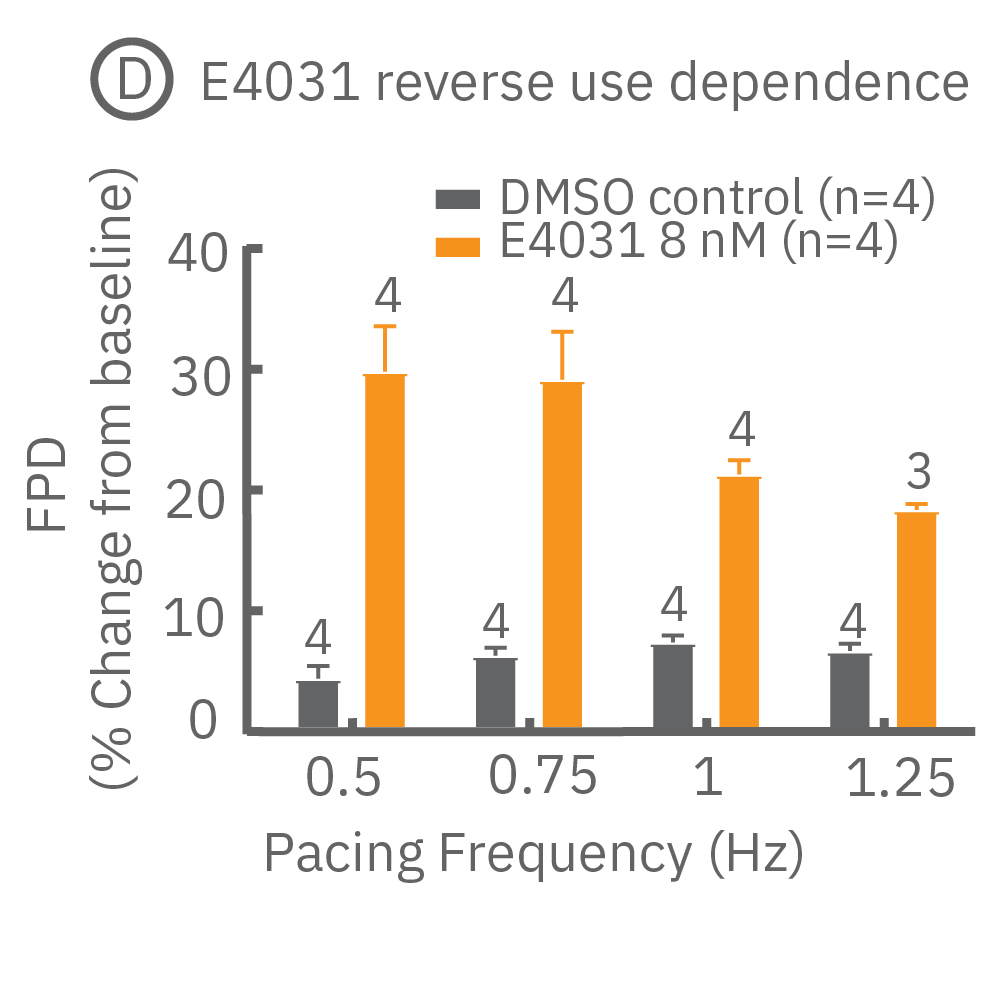
(D) Pluricyte® 心筋細胞を異なる刺激頻度でペーシングし、E4031 (hERG チャネルブロッカー、オレンジ色)とDMSO (グレー色)を投与してFPDを測定した。E4031 投与時、FPDはペーシングレートの上昇に伴い減少し、その逆使用依存性が示された。
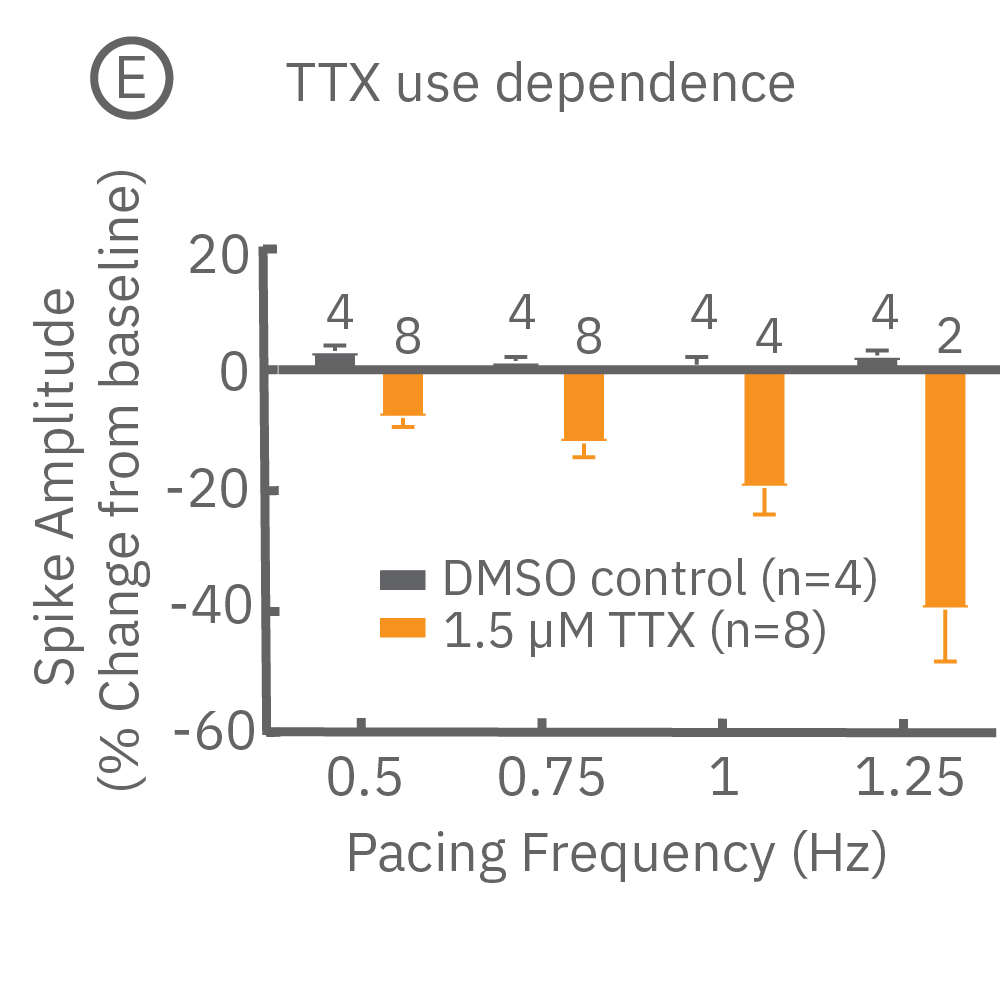
(E) 同様に Pluricyte ® 心筋細胞ペーシング下で、TTX (ナトリウムチャネルブロッカー,オレンジ色) と DMSO (グレー色)を投与した際の 脱分極スパイクの変化を示す。TTX 投与時、スパイク振幅値はペーシング頻度上昇に伴い減少し、その逆使用依存性が示された。
(D,E 共に、バーは平均値の標準誤差、棒グラフ上の数値はペーシングに成功したwell数を示す。)
ペーシングによるFPD-拍動間隔相関の検証
心筋細胞の再分極は本質的に拍動頻度に伴い変化します。一方で、それぞれの薬物に対する反応は極めて敏感です。本事例では、オプトジェネティクス刺激により拍動頻度を一定に保ちながら、FPDを測定しました。
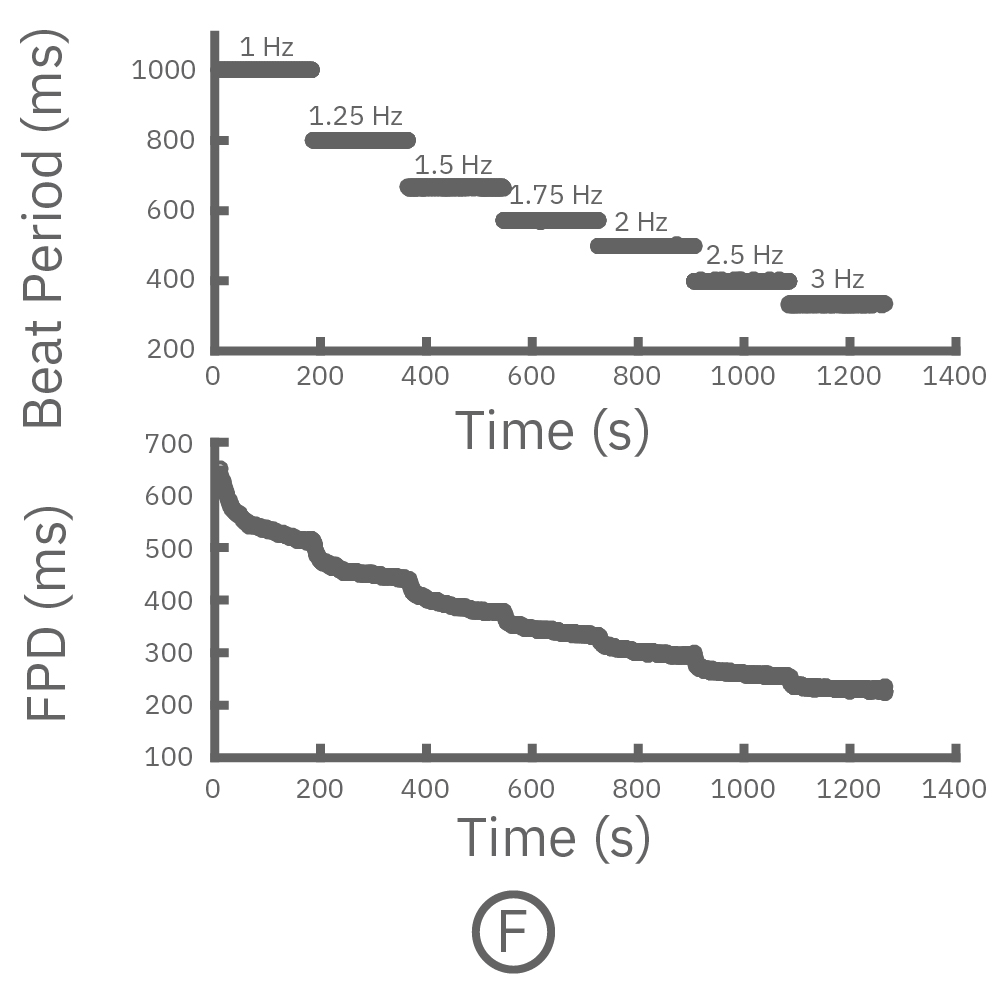
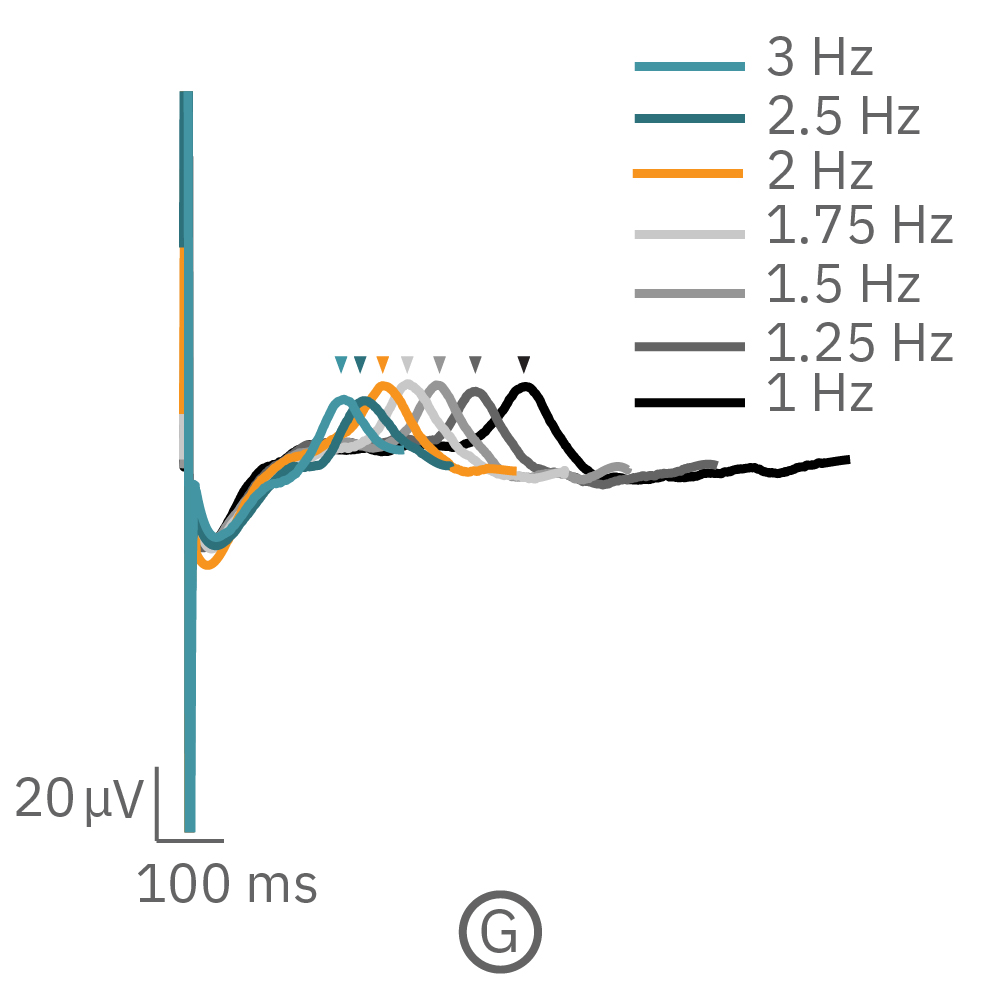
(F,G) Pluricyte® 心筋細胞にペーシングを印加し、ペースレートを段階的に上昇させた(Chirp アッセイ)。F下段は~3Hz のペーシング下において、各拍動レート毎に得られた Field Potential Duration (FPD) を示す。Gは各拍動レートから得られた波形を示す。
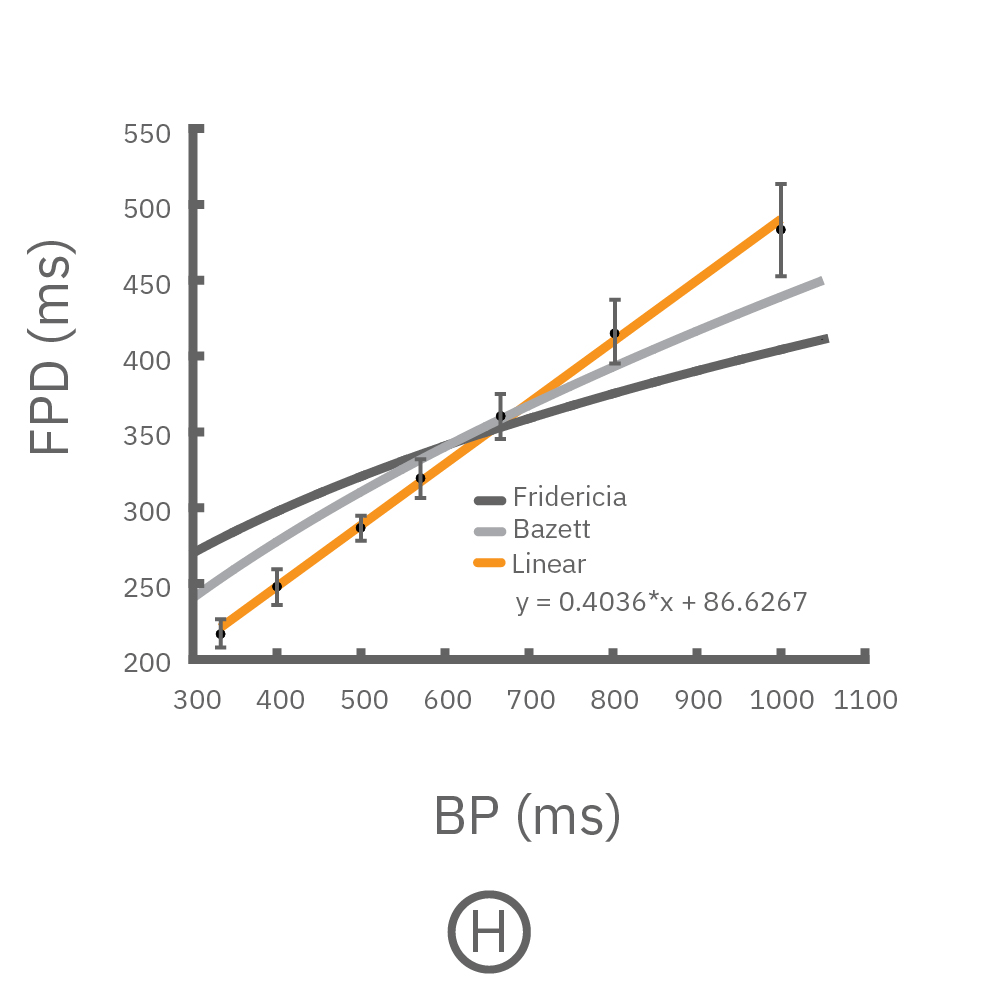
(H) 臨床で用いられる典型的な補正式 (Fridercia、Bazzett)によるFPD-拍動間隔の相関(グレー)と LUMOS 光刺激装置による光刺激による相関(オレンジ)を示す。光刺激により、補正式よりも正確な相関が示された。
ペーシングによる不整脈リスクの定量化
本事例では、光刺激により拍動レートをコントロールし、拍動レート依存性を排除した不整脈リスクの定量化を検証しました。
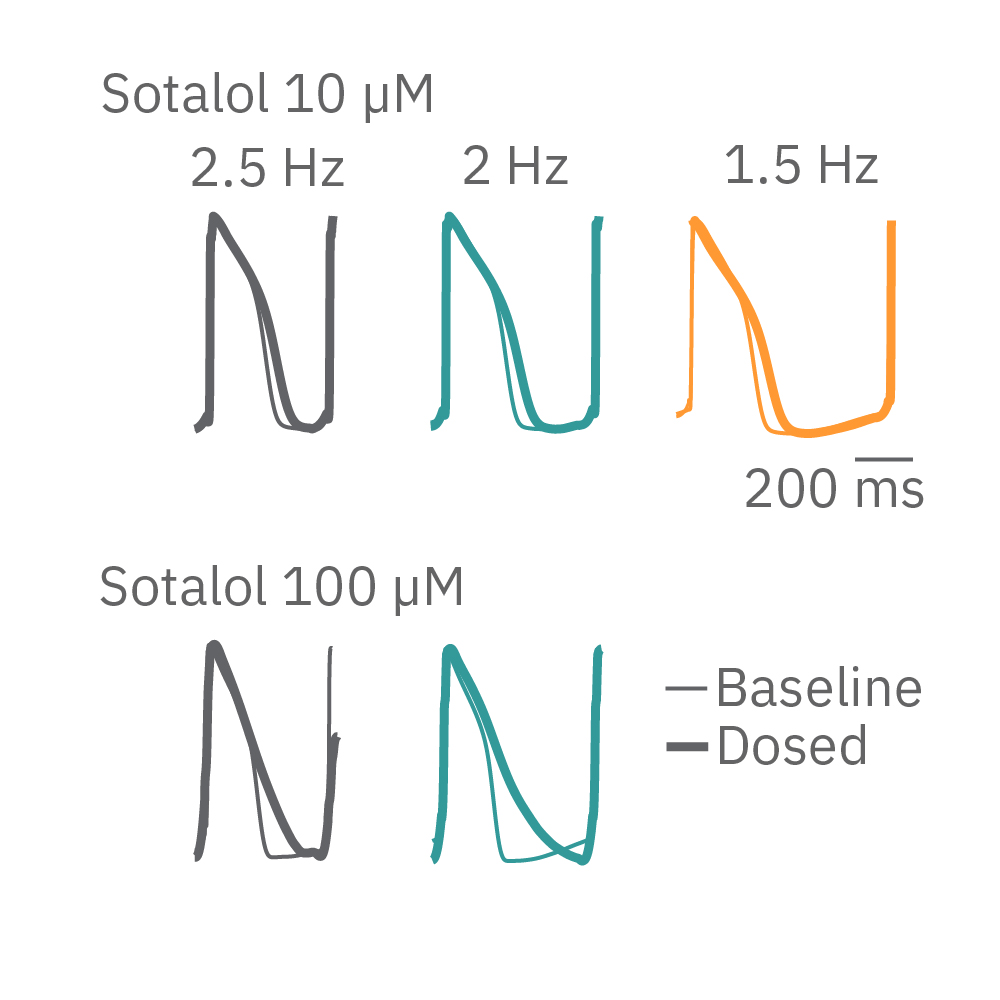
ヒトiPS細胞由来心筋細胞にチャネルロドプシン2 (ChR2) を導入し、光刺激装置 LUMOS で青色の光を照射し、異なるレートでペーシングした。各拍動レート毎にソタノールを投与したところ、APDの遅延は拍動レートの遅延に相関し、その逆使用依存性が示された。
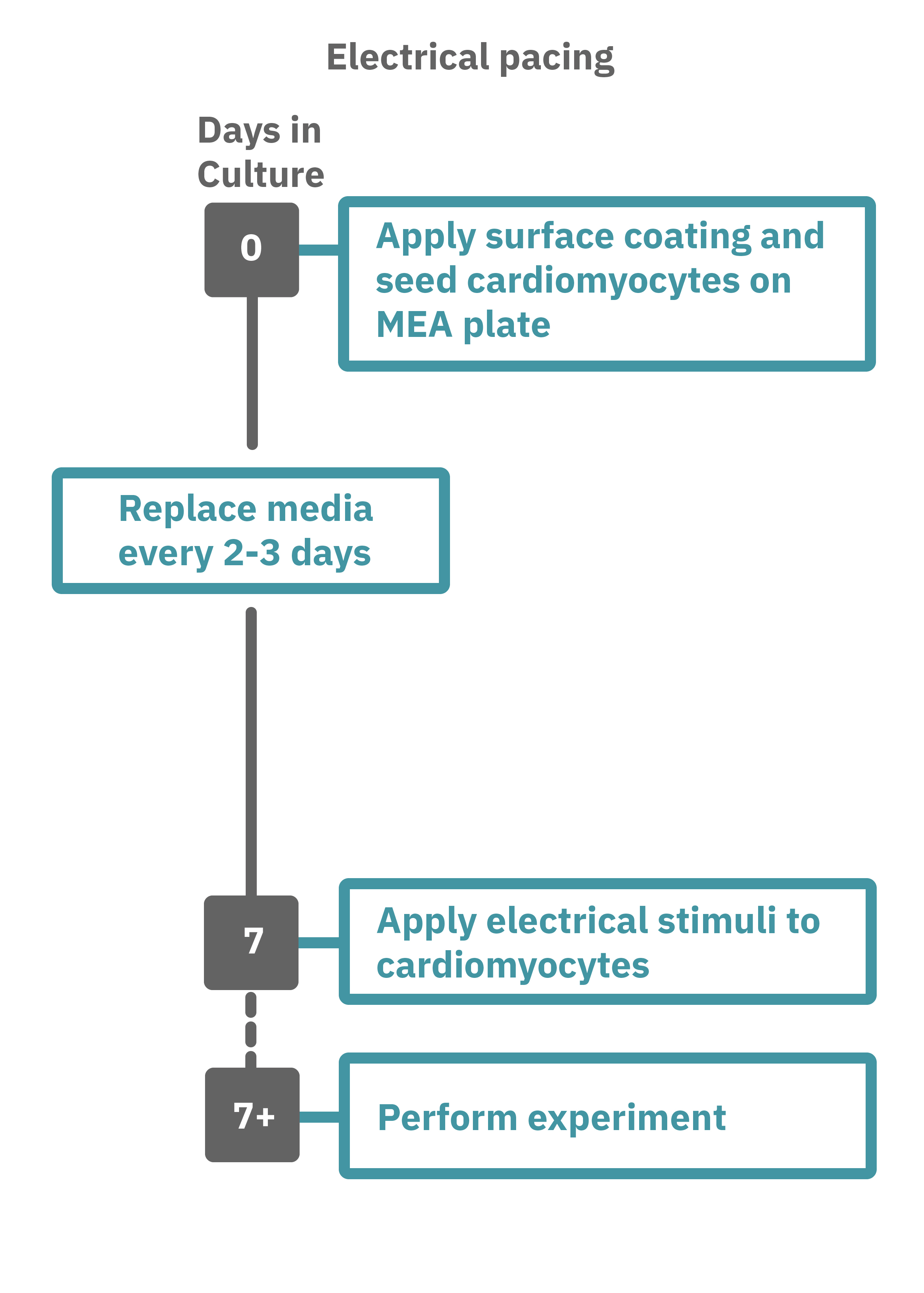
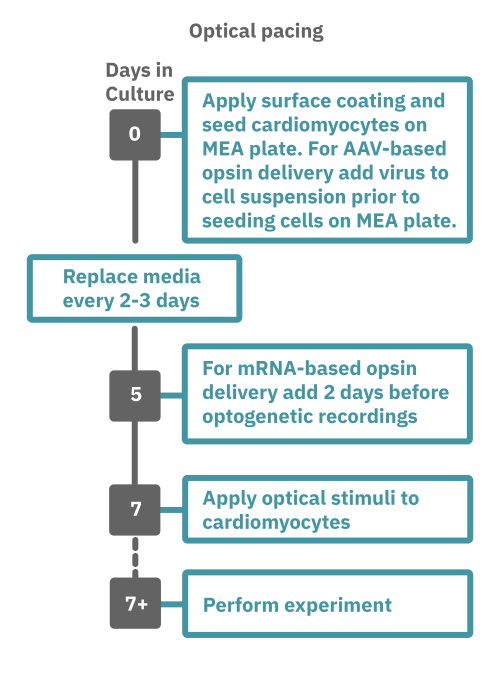
Maestro Pro/Edge による心筋細胞ペーシングアッセイは非常に簡単です。
コーティングされたMEAプレート上に心筋細胞を播種します (Day 0)。オプトジェネティクス試験においては、細胞播種時に、アデノ随伴ウイルスベクター(AAVベクター)を用いてウィルスを細胞懸濁液に添加します。オプシンの発現には7-14 日を要します。心筋細胞にmRNAベースのオプシンを導入する場合は、心筋細胞の活動ピーク時に導入し、オプシンの発現を2日間待ちます。
データ測定日 (例: Day 7+) にプレートを Maestro に搭載し測定を行います。光刺激装置 LUMOSを用いて光刺激を印加 (或いは Maestro 内蔵電気刺激装置を用いて電気刺激を印加)します。測定されたデータは付属のソフトで解析可能です。

Maestro MEA による心筋細胞ペーシングアッセイ:特徴
- 電気刺激 - Maestro MEAプレート上の全電極から電気刺激の印加が可能です。刺激の印加やコントールは Axis Navigator ソフトウエア上で簡単に行えます。アーチファクト除去機能で、取得データの解析も容易です。
- 光刺激 - Maestro Pro/Edge での光刺激には、光刺激装置 LUMOS (特許取得) がご使用頂けます。各 well 毎の刺激強度、持続時間、波長のコントロールが可能です。
- 1システムで4種類のアッセイ - Maestro Pro/Edgeでは、1枚のプレートで次の4種類のアッセイが行えます。[1] 細胞外電位応答 [2] シグナル伝播 [3] Contractility (弛緩収縮評価) [4] LEAP (Action Potential 形態シグナル)
- ラベルフリー・リアルタイムで細胞の電気的な活動を測定 - プレート上の電極を用いて心筋細胞の活動電位を測定します。ラベルフリー、リアルタイムな測定は、試薬など2次的要因によるゆがみがなく、細胞の変化をより正確にとらえます。また、数日から数週間に渡る慢性評価にも最適です。
- 同一プレート上で培養から測定まで - MEAプレート上で直接細胞を培養し、測定します。環境要因による変化を最小限にとどめながら、細胞への負担が少ない状態で、細胞の変化を検出することができます。
- 安定した環境下での実験 - 温度・CO₂ 濃度は、装置搭載のコントローラで自動制御されます。また、Maestro は外来ノイズ・振動に影響されにくい設計になっています。安定した環境で毎日安心して実験に望めます。
- 簡単操作 - 電気生理未経験の方でも簡単に実験が行えます。MEAプレート上に細胞を培養し、装置に搭載するだけで、心筋細胞の電気的な活動の測定が可能です。付属のソフトウエアパッケージを用いて、数クリックで複数の指標に基づいた解析結果が得られ、結果の作表まで行うことができます。

Cardiac MEA
Show Full DetailsWhat is Cardiac MEA
Cardiac MEA (microelectrode array) technology is a label-free method for recording electrical activity in heart cells. Tiny electrodes embedded in the culture surface detect electrical signals from cardiomyocytes, allowing continuous, noninvasive monitoring of cardiac function in real time. This technology provides insights into cardiomyocyte function, rhythm, and drug response in 2D and 3D cell models
Why Cardiac MEA matters
Traditional cardiac assays rely on indirect, low resolution, or endpoint measurements that fail to capture electrical function, rhythm changes, and time-dependent drug effects. Cardiac MEA technology addresses this gap by providing direct, physiologically relevant measurements of cardiac electrophysiology, supporting safer drug development, improved cardiotoxicity screening, and more predictive disease models.

Contractility
Show Full DetailsWhat is Contractility?
Every beat of the heart is characterized by a contraction of the heart that pumps the blood out to the body. When cardiomyocytes are cultured on top of electrodes, they form a spontaneously beating syncytium. With each beat, the cells contract and relax, changing their shape and coverage over the electrodes. These changes can be measured as a change in impedance, or contractility.
Why Contractility Matters
Contractility is often used to characterize the mechanical properties of induced pluripotent stem cell-derived cardiomyocytes and to detect the effects of compounds on cardiac contractile function (e.g., inotropes). Measures such as beat amplitude, beat period, and excitation-contraction delay reveal changes in contractile function due to cardiomyocyte maturation or compound addition.

Optogenetics
Show Full DetailsWhat is Optogenetics?
Optogenetics is a technique that involves the use of light to control cell function. Cells are first genetically modified to express light-sensitive ion channels, called opsins. Then, light can be used to activate the opsin. The most well-known opsins are light-gated ion channels that can control the excitability of the cell membrane.
Why Optogenetics Matters
By delivering precise, time-locked stimulation, optogenetics enables researchers to interrogate circuit behavior, model disease-related dysfunction, and evaluate therapeutic interventions with high temporal and spatial resolution.









